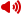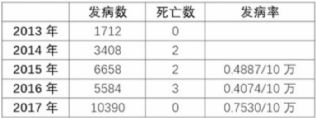
长春长生问题疫苗事件曝光
国家药监局7月15日通告,国家食品药品监督局开展飞行检查,发现长春长生冻干人用狂犬病疫苗生产存在记录造假等行为。目前,吉林省药监局已收回长春长生《药品GMP 证书》,同时长春长生已被要求停止狂犬疫苗的生产。
这之后的第三天,也就是7月18日,吉林省药监局公布,该公司2017年11月生产的25万支百白破疫苗效价不合格,按劣药处理,罚款344万。
22日晚,李克强总理就疫苗事件作出批示:此次疫苗事件突破人的道德底线,必须给全国人民一个明明白白的交代。
同日早些时候,国家药监局负责人也就此事进行了通报,表示会同吉林省局已对企业立案调查,涉嫌犯罪的移送公安机关追究刑事责任。
河北:不合格百白破疫苗流向石家庄、廊坊和定州三市。
广东:并未购进涉事批次疫苗。
北京:未采购长春长生两款问题疫苗。
浙江:未发现问题疫苗流入。上海:已全面停用长春长生狂犬病疫苗。
河南:暂停使用、就地封存所有长春长生的狂犬病疫苗。海南:已全面停用长春长生狂犬病疫苗。重庆:暂停使用并就地封存长春长生狂犬病疫苗。山西:已停止使用长春长生狂犬病疫苗。
7月19日,山西省疾病预防控制中心官方网站发布消息称,根据国家药品监督管理局的通告和长春长生生物科技有限责任公司紧急通知,全省各接种点已停止使用长春长生狂犬病疫苗。
广西:已有58个县(市、区)召回93384支。
福建:没有涉事批次狂犬疫苗未采购不合格百白破疫苗。
青海:暂未回应是否有相关问题疫苗流入。
湖南:境内没有涉事疫苗。
江苏:疫苗都是通过批签发检验、审核合格统一招标采购。
西藏:未采购问题疫苗。
陕西:不合格批次百白破未采购。
天津:未采购长春长生狂犬病疫苗。
四川:问题冻干人用狂犬病疫苗已全部实施召回,并未进入社会。
江西:未采购涉事批次疫苗。
安徽:长春长生公司狂犬疫苗全面停用,问题百白破疫苗未流入。